对甲基苯基磺酰氯
| 对甲基苯基磺酰氯 | |
|---|---|
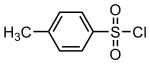
| |

| |
| IUPAC名 4-甲基苯磺酰氯 | |
| 别名 | p-TsCl, TsCl |
| 识别 | |
| CAS号 | 98-59-9 |
| ChemSpider | 7119 |
| SMILES |
|
| InChI |
|
| InChIKey | YYROPELSRYBVMQ-UHFFFAOYAN |
| 性质 | |
| 化学式 | C7H7ClO2S |
| 摩尔质量 | 190.65 g·mol⁻¹ |
| 外观 | 白色固体 |
| 熔点 | 65-69 °C |
| 沸点 | 134 °C at 10 mmHg |
| 溶解性(水) | 水解 |
| 危险性 | |
| 主要危害 | 释放氯化氢 |
| NFPA 704 | |
| 闪点 | 128 °C |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
对甲苯磺酰氯(4-甲基磺酰氯,常简写为:TosCl或TsCl)是一种分子式为CH3C6H4SO2Cl的有机化合物。该化合物为有恶臭味的白色固体试剂,并广泛的应用于有机合成[1]。该化合物属于甲苯和磺酰氯官能团的衍生物。
应用
[编辑]该化合物的特点是能够转化醇(ROH)为相应的对甲苯磺酸酯(ROTs),或对甲苯磺酸酯的衍生物(英文:tosylate):
- CH3C6H4SO2Cl + ROH → CH3C6H4SO2OR + HCl
对甲苯磺酸酯可通过氢化锂铝发生裂解反应:
- 4 CH3C6H4SO2OR + LiAlH4 → LiAl(O3SC6H4CH3)4 + 4 RH
因此,上述两个反应可成为脱去羟基的一种方法。
- CH3C6H4SO2Cl + R2NH → CH3C6H4SO2NR2 + HCl
得到的磺酰胺化合物不具碱性,甚至伯胺生成的磺酰胺是显弱酸性的。
制备对甲苯磺酸酯和对甲苯磺酰酰胺时,反应条件都有碱的参与,其作用是缚酸剂。其中碱的选择对于对甲苯磺酰化非常重要,典型的碱包括:吡啶和三乙胺。另外还有一些不太常用的碱,如催化量的三甲基氯化铵和三乙胺反应生成的三甲胺也是一种高效的碱[1]。
在多肽的合成中,氨基酸被一个个添加到肽链上使得肽链延长,对甲苯磺酰氯可被用来保护这些氨基酸的氨基:
- HOOC-CH2-NH2 + Tos-Cl → HOOC-CH2-NH-Tos
氨基被保护的氨基酸的羧基可以在脱水剂(如DCCD)的作用下与肽链游离氨基之间脱水,从而形成新的肽键;氨基上的Tos基可以用钠氨还原的方式被除去,重新形成游离的氨基;可以进行下一个肽键的合成,如此循环操作得到整条肽链。故对甲苯磺酰氯在此的作用就是使得氨基钝化,防止相同氨基酸的羧基氨基之间漫无目的地脱水,避免了大量副反应的产生。然而现在在肽链合成方面最常用的氨基保护基是9-芴甲氧羰基(Fmoc)。
其他反应
[编辑]作为一个应用广泛的试剂,对甲苯磺酰氯在多种化学反应当中被认为都具有很强的活性。它还可应用于脱水剂以制备腈,异腈,二亚胺[1]。 在一些不常见的反应中,锌可还原对甲苯磺酰氯为亚磺酸盐,CH3C6H4SO2Na[3]。
工业生产
[编辑]对甲苯磺酰氯在实验室合成中并不昂贵,因为它是工业生产邻甲苯磺酰氯(一种生产糖精的原料)时的一种副产物,反应通过甲苯发生氯磺酰化进行: [4]
- CH3C6H5 + SO2Cl2 → CH3C6H4SO2Cl + HCl
参考文献
[编辑]- ^ 1.0 1.1 1.2 D. Todd Whitaker, K. Sinclair Whitaker, Carl R. Johnson, Julia Haas, "p-Toluenesulfonyl Chloride" in Encyclopedia of Reagents for Organic Synthesis, 2006, John Wiley, New York. doi:10.1002/047084289X.rt136.pub2 Article Online Posting Date: September 15, 2006
- ^ Junji Ichikawa, Ryo Nadano, Takashi Mori, and Yukinori Wada (2006). "5-endo-trig Cyclization of 1,1-Difluoro-1-alkenes: Synthesis of 3-Butyl-2-Fluoro-1-Tosylindole". Org. Synth..
- ^ Frank C. Whitmore, Frances H. Hamilton (1941). "Sodium Toluenesulfinate". Org. Synth.; Coll. Vol. 1: 492.
- ^ Otto Lindner, Lars Rodefeld "Benzenesulfonic Acids and Their Derivatives" in Ullmann's Encyclopedia of Industrial Chemistry 2001, Wiley-VCH, Weinheim. Published online: 15 September, 2000

