丁炔二酸二甲酯
外观
| 丁炔二酸二甲酯 | |
|---|---|

| |
| |
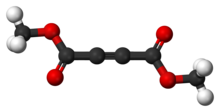
| IUPAC名 Dimethyl acetylenedicarboxylate | |
| 别名 | DMAD Acetylenedicarboxylic acid, dimethyl ester |
| 识别 | |
| CAS号 | 762-42-5 |
| ChemSpider | 12440 |
| SMILES |
|
| InChI |
|
| InChIKey | VHILMKFSCRWWIJ-UHFFFAOYAX |
| RTECS | ES0175000 |
| 性质 | |
| 化学式 | C6H6O4 |
| 摩尔质量 | 142.11 g·mol⁻¹ |
| 外观 | 无色液体 |
| 密度 | 1.1564 g/cm³ |
| 熔点 | °C |
| 沸点 | 195–198 °C 96–98°C(8 mm Hg) |
| 溶解性(水) | 不溶 |
| 溶解性(其他溶剂) | 溶于多数有机溶剂 |
| 折光度n D |
1.447 |
| 结构 | |
| 偶极矩 | 0 D |
| 危险性 | |
| 警示术语 | R:R34 |
| 安全术语 | S:S23 S26 S27 S36/37/39 S45 |
| 主要危害 | 有毒气体 |
| 闪点 | 187 °F |
| 相关物质 | |
| 相关化学品 | 丙炔酸甲酯、 六氟代-2-丁炔、 乙炔 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
丁炔二酸二甲酯(英文缩写DMAD)是丁炔二酸与甲醇形成的羧酸酯,结构简式为CH3O2CC2CO2CH3。这种酯在常温常压下以液态存在,具有很强的亲电活性。因此,丁炔二酸二甲酯在实验室中广泛用作环加成反应(例如Diels-Alder反应)的亲双烯体。它也是一种活泼的Michael加成反应的受体。[1][2]
制备
[编辑]尽管现在丁炔二酸二甲酯可以廉价获得,它依旧是用最早的方法制备的。首先将顺丁烯二酸溴化得到二溴丁二酸,然后在氢氧化钾作用下发生脱卤化氢反应生成丁炔二酸。[3][4]丁炔二酸最后与甲醇在硫酸催化下发生酯化反应得到丁炔二酸二甲酯:[5]
应用
[编辑]早期曾利用环庚三烯与丁炔二酸二甲酯的加合物作为亚甲基供体,与乙炔反应用于合成环丙烯的衍生物。环庚三烯在反应后转变为少一个碳的苯。
丁炔二酸二甲酯与苯发生光化学反应可以扩环,生成1,3,5,7-环辛四烯-1,2-二羧酸甲酯的两种同分异构体。[6]
正十二面体烷的全合成也多次使用丁炔二酸二甲酯,例如2到3的反应是二氢富瓦烯与丁炔二酸二甲酯的Diels-Alder反应。
也可用于合成吡啶或嘧啶等杂环,例如HIV整合酶抑制剂Raltegravir的起始原料:[7]
安全
[编辑]参考资料
[编辑]- ^ Stelmach, J. E.; Winkler, J. D. “Dimethyl Acetylenedicarboxylate” in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. DOI: 10.1002/047084289.
- ^ Sahoo, Manoj. Dimethyl Acetylene Dicarboxylate. Synlett. 2007, 2007: 2142. doi:10.1055/s-2007-984894.
- ^ Bandrowski, E. Ueber Acetylendicarbonsäure. Berichte der deutschen chemischen Gesellschaft. 1877, 10: 838. doi:10.1002/cber.187701001231.
- ^ Abbott, T. W.; Arnold, R. T.; Thompson, R. B.. "Acetylenedicarboxylic acid". Org. Synth.; Coll. Vol. 2: 10.
- ^ Huntress, E. H. Lesslie, T. E.; Bornstein, J.. "Dimethyl Acetylenedicarboxylate". Org. Synth.; Coll. Vol. 4: 329.
- ^ Grovenstein, Erling; Campbell, Thomas C., Shibata, Tomoo. Photochemical reactions of dimethyl acetylenedicarboxylate with benzene and naphthalene. The Journal of Organic Chemistry. 1969-07-31, 34 (8): 2418–2428. doi:10.1021/jo01260a035.
- ^ Vincenzo Summa, Alessia Petrocchi,Fabio Bonelli,Benedetta Crescenzi,Monica Donghi,Marco Ferrara,Fabrizio Fiore,Cristina Gardelli,Odalys Gonzalez Paz,Daria J. Hazuda,Philip Jones,Olaf Kinzel,Ralph Laufer,Edith Monteagudo,Ester Muraglia,Emanuela Nizi,Federica Orvieto,Paola Pace,Giovanna Pescatore,Rita Scarpelli,Kara Stillmock,Marc V. Witmer,Michael Rowley. Discovery of Raltegravir, a Potent, Selective Orally Bioavailable HIV-Integrase Inhibitor for the Treatment of HIV-AIDS Infection. The Journal of Medicinal Chemistry. 2008-09-03, 51: 5843 – 5855. doi:10.1021/jm800245z.



