价层电子对互斥理论
价层电子对互斥理论(英语:Valence Shell Electron Pair Repulsion,简称为VSEPR),是一个用来预测单个共价分子形态的化学模型。理论通过计算中心原子的价层电子数和配位数来预测分子的几何构型,并构建一个合理的路易斯结构式来表示分子中所有键和孤对电子的位置。
价层电子对互斥理论也称为吉莱斯皮-尼霍姆理论,因为该理论的两位主要创始人分别是罗纳德·吉莱斯皮和罗纳德·尼霍姆。
历史
[编辑]1939 年,日本化学家槌田·龙太郎(Ryutaro Tsuchida)首先提出分子结构与价层电子对数量之间关系[1]。
1940年,由内维尔·席德维克和 赫伯特·包维尔(Herbert Powell)在牛津大学的贝克奖获奖讲座上独立提出[2]。
1957 年,伦敦大学学院的罗纳德·吉莱斯皮和罗纳德·尼霍姆将这一概念提炼为更详细的理论[3][4]。
理论基础
[编辑]价层电子对互斥理论的基础是,分子或离子的几何结构主要决定于与中心原子相关的电子对之间的排斥作用。该电子对既可以是成键的,也可以是没有成键的(叫做孤对电子)。只有中心原子的价电子才能够对分子的形状产生有意义的影响。
分子中电子对间的排斥的三种情况为:
- 孤对电子间的排斥(孤-孤排斥);
- 孤对电子和成键电子对之间的排斥(孤-成排斥);
- 成键电子对之间的排斥(成-成排斥)。
分子会尽力避免这些排斥来保持稳定。当排斥不能避免时,整个分子倾向于形成排斥最弱的结构(与理想形状有最小差异的方式)。
孤对电子间的排斥被认为大于孤对电子和成键电子对之间的排斥,后者又大于成键电子对之间的排斥。因此,分子更倾向于最弱的成-成排斥。
配体较多的分子中,电子对间甚至无法保持90°的夹角,因此它们的电子对更倾向于分布在多个平面上。
空间位数
[编辑]
分子的空间位数(steric number)是指其中心原子键结原子的个数(σ键)加上中心原子的孤电子对数量。空间位数常用在价层电子对互斥理论(VSEPR)中确认分子的形状,也会用在分子结构研究中。
在用VSEPR理论预测分子形状时,计算空间位数是其中的一个重要步骤。例如针对分子四氟化硫,中心的硫原子有四个配体,因此其配位数为4。但中央原子仍留有一对孤电子对,因此其空间位数是5。有了中心原子的空间位数配合其孤电子对数,就可以预测其分子形状。
实际预测
[编辑]下面是价层电子对互斥理论预测的分子形状表。
| 电子对数 | 杂化类型(混层类型) | 轨道形状 | 单电子对数(孤电子对) | 分子形状 | 例 |
|---|---|---|---|---|---|
| 2 | sp | 直线形 | 0 | 直线形 | BeCl2、CO2 |
| 3 | sp2 | 平面正三角形 | 0 | 平面正三角形 | BCl3 |
| 1 | V字形(角形、弯曲形) | SO2 | |||
| 4 | sp3 | 正四面体 | 0 | 正四面体 | CH4 |
| 1 | 三角锥 | NH3 | |||
| 2 | V字形(角形、弯曲形) | H2O | |||
| 5 | sp3d | 三角双锥 | 0 | 三角双锥 | PCl5 |
| 1 | 变形四面体(跷跷板形) | TeCl4 | |||
| 2 | T字形 | ClF3 | |||
| 3 | 直线形 | I3− | |||
| 6 | sp3d2 | 正八面体 | 0 | 正八面体 | SF6 |
| 1 | 四方锥 | IF5 | |||
| 2 | 平面十字形 | ICl4− | |||
| 3 | T字形 | ||||
| 4 | 直线形 | ||||
| 7 | sp3d3 | 五角双锥 | 0 | 五角双锥 | IF7 |
| 1 | 五角锥 | ||||
| 2 | 五角形 |
下图中,价壳层电子对互斥理论常用AXE方法计算分子构型。这种方法也叫ABE,其中A代表中心原子,X或B代表配位原子,E代表孤电子对。
| 电子对数 | 没有孤电子对 (基本形状) |
1个孤电子对 | 2个孤电子对 | 3个孤电子对 |
|---|---|---|---|---|
| 2 | 直线形 |
|||
| 3 |  平面三角形 |
 角形 |
||
| 4 | 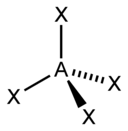 四面体形 |
 三角锥形 |
 角形 |
|
| 5 |  三角双锥形 |
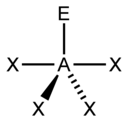 变形四面体形 |
 T字形 |
 直线形
|
| 6 |  八面体形 |
 四角锥形 |
 平面四方形 |
|
| 7 |  五角双锥形 |
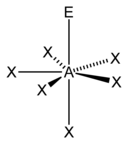 五角锥形 |
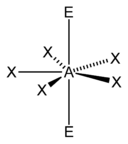 平面五角形 |
|
| 8 |
下图中:孤电子对以淡黄色球体表示。分子形状为实际几何构型,即不包含孤对电子的构型。
| 分子类型 | 分子形状 | 中心原子价电子对的排布方式† | 分子的几何构型‡ | 实例 |
|---|---|---|---|---|
| AX1En | 双原子分子 (直线形) |
HF、O2 | ||
| AX2E0 | 直线形 | BeCl2、HgCl2、CO2 | ||
| AX2E1 | 角形 | 
|

|
NO2−、SO2、O3 |
| AX2E2 | 角形 | 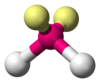
|

|
H2O、OF2 |
| AX2E3 | 直线形 | 
|
XeF2、I3− | |
| AX3E0 | 平面三角形 | 
|

|
BF3、CO32−、NO3−、SO3 |
| AX3E1 | 三角锥形 | 
|

|
NH3、PCl3 |
| AX3E2 | T字形 | 
|

|
ClF3、BrF3 |
| AX4E0 | 四面体形 | 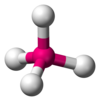
|

|
CH4、PO43−、SO42−、ClO4− |
| AX4E1 | 变形四面体形 | 
|
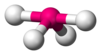
|
SF4 |
| AX4E2 | 平面四方形 | 
|

|
XeF4 |
| AX5E0 | 三角双锥形 | 
|

|
PCl5 |
| AX5E1 | 四角锥形 | 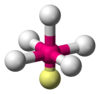
|

|
ClF5、BrF5 |
| AX5E2 | 平面五角形 | 
|

|
XeF 5- |
| AX6E0 | 八面体形 | 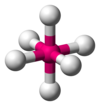
|

|
SF6 |
| AX6E1 | 五角锥形 | 
|

|
XeOF 5−、IOF 52− [5] |
| AX7E0 | 五角双锥形 | 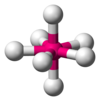
|

|
IF7 |
| AX8E0 | 四方反棱柱形 | 
|

|
XeF2− 8, ZrF84-, ReF8- |
| AX9E0 | 三侧锥三角柱 | 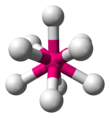
|

|
ReH2− 9 |
范例
[编辑]甲烷分子(CH4)是四面体结构,是一个典型的AX4型分子。中心碳原子周围有四个电子对,四个氢原子位于四面体的顶点,键角(H-C-H)为109°28'。
一个分子的形状不但受配位原子影响,也受孤对电子影响。氨分子(NH3)中心原子杂化类型与甲烷相同(sp3),分子中有四个电子云密集区,电子云分布依然呈四面体。其中三个是成键电子对,另外一个是孤对电子。虽然它没有成键,但是它的排斥力影响著整个分子的形状。因此,这是一个AX3E型分子,整个分子的形状是三角锥形,因为孤对电子是不可“见”的。
事实上,电子对数为七是有可能的,轨道形状是五角双锥。但是它们仅存在于不常见的化合物之中,比如在六氟化氙中,有一对孤电子,它的构型趋向于八面体结构,因为孤对电子倾向于位于五角形的平面上。另一个例子为七氟化碘,碘没有孤电子,七个氟原子呈五角双锥状排列。
电子对数为八也是有可能的,这些化合物一般为四方反棱柱体结构,[6] 例子有八氟合氙酸亚硝酰中的 [XeF8]2− 离子[7][8] 以及八氰合钼(Ⅳ)阴离子 [Mo(CN)8]4− 和八氟合锆(Ⅳ)阴离子 [ZrF8]4−。
例外
[编辑]在一些化合物中VSEPR理论不能正确的预测分子空间构型。
过渡金属化合物
[编辑]许多过渡金属化合物的几何构型不能用VSEPR理论解释,可以归结于价层电子中没有孤对电子以及核心的d电子与配体的相互作用。[9] 这些化合物的结构可以用VALBOND理论预测,包括金属氢化物和烷基配合物(例如六甲基钨),这个理论的基础是sd 杂化轨道和三中心四电子键模型。[10][11] 晶体场理论是另一个经常可以解释配合物几何构型的理论。
IIA族卤化物
[编辑]较重碱土金属的三原子卤化物的气相结构(例如:钙、锶、钡的卤化物,MX2)并不像预测的那样为直线形,而是V形。(X-M-X的大致键角: CaF2,145°;SrF2,120°;BaF2,108°;SrCl2,130°;BaCl2,115°;BaBr2,115°;BaI2,105°)。[12] 罗纳德·吉莱斯皮提出这是因为配体与金属原子的内层电子发生相互作用,极化使得内层电子云不是完全球面对称,因此导致了分子结构的变化。[9][13]
AX2E0型分子
[编辑]根据计算,较重的碳族元素炔烃类似物(RM≡MR,其中M = Si、Ge、Sn、Pb)的结构是角形。[14][15][16]
AX2E2型分子
[编辑]一个例子是氧化锂分子,即Li2O,它的中间构型是直线形而不是弯曲的,这一点可以归结于如果构型是弯曲的,锂原子之间将产生强烈的排斥作用。[17]
另一个例子是O(SiH3)2(二甲硅醚)的Si-O-Si键的键角为144.1°,与其他分子中的键角相比差别较大,比如Cl2O (110.9°)、(CH3)2O (111.7°)以及N(CH3)3 (110.9°)。格莱斯皮的合理解释是孤对电子的位置不同。当配体的电负性与中心原子类似或更大时,孤对电子有能力排斥其他电子对,导致键角较小。 [9] 当中心原子电负性较大时,就像O(SiH3)2中,孤对电子的定域不明显,排斥作用较弱,这种结合导致了强配体之间的排斥(-SiH3与上面的例子相比是一个比较大的配体),使得Si-O-Si键的键角比预想的要大。[9]
一些形如AX6E1的分子
[编辑]一些AX6E1型分子,例如含有Te(IV)或Bi(III)离子的化合物如TeCl62−、TeBr62−、BiCl63−、BiBr63−和BiI63−是正八面体结构;其孤对电子并不影响其构型[18]。 一种合理化解释是因为配体原子排列的拥挤没有给孤对电子留下空间[9];另一种合理化解释是惰性电子对效应。[19]
与其他相关理论的对比
[编辑]价层电子对互斥理论、价键理论和分子轨道理论都是关于分子如何构成的理论。价键理论主要关注于σ键和π键的形成,通过研究受成键情况影响的轨道形状描述分子的形状。价键理论也会借助VSEPR。分子轨道理论则是关于原子和电子是如何组成分子或多原子离子的一个更精密的理论。
参考资料
[编辑]- ^ 龙太郎, 槌田. 新簡易原子價論. 日本化学会志. 1939, 60 (3) [2024-04-13]. doi:10.1246/nikkashi1921.60.245. (原始内容存档于2024-06-03).
- ^ Bakerian Lecture: Stereochemical types and valency groups. Proceedings of the Royal Society of London. Series A. Mathematical and Physical Sciences. 1940-10-09, 176 (965) [2024-04-13]. ISSN 0080-4630. doi:10.1098/rspa.1940.0084. (原始内容存档于2022-07-03) (英语).
- ^ Gillespie, R. J.; Nyholm, R. S. Inorganic stereochemistry. Quarterly Reviews, Chemical Society. 1957-01-01, 11 (4) [2024-04-13]. ISSN 0009-2681. doi:10.1039/QR9571100339. (原始内容存档于2024-06-15) (英语).
- ^ Gillespie, R. J. The electron-pair repulsion model for molecular geometry. Journal of Chemical Education. 1970-01, 47 (1) [2024-04-13]. ISSN 0021-9584. doi:10.1021/ed047p18. (原始内容存档于2023-02-11) (英语).
- ^ Baran, E (2000). "Mean amplitudes of vibration of the pentagonal pyramidal XeOF5− and IOF52− anions". Journal of Fluorine Chemistry 101: 61. doi:10.1016/S0022-1139(99)00194-3.
- ^ Wiberg, Egon; Wiberg, Nils. Inorganic Chemistry. Arnold Frederick Holleman. Academic Press. 2001: 1165. ISBN 0123526515.
- ^ Peterson, S. W.; Holloway, J. H.; Coyle, B. A.; Williams, J. M. Antiprismatic Coordination about Xenon: The Structure of Nitrosonium Octafluoroxenate(VI). Science. 1971-09-24, 173 (4003): 1238–1239 [2022-04-04]. ISSN 0036-8075. doi:10.1126/science.173.4003.1238. (原始内容存档于2022-04-04) (英语).
- ^ Hanson, Robert M. Molecular origami: precision scale models from paper. University Science Books. 1995. ISBN 093570230X.
- ^ 9.0 9.1 9.2 9.3 9.4 Models of molecular geometry, Gillespie R. J., Robinson E.A. Chem. Soc. Rev., 2005, 34, 396–407, doi: 10.1039/b405359c
- ^ Landis, C. K.; Cleveland, T.; Firman, T. K. Making sense of the shapes of simple metal hydrides. J. Am. Chem. Soc. 1995, 117, 1859–1860.
- ^ Landis, C. K.; Cleveland, T.; Firman, T. K. Structure of W(CH3)6. Science 1996, 272, 182–183.
- ^ Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements 2nd. Oxford:Butterworth-Heinemann. 1997. ISBN 0-7506-3365-4.
- ^ Core Distortions and Geometries of the Difluorides and Dihydrides of Ca, Sr, and Ba Bytheway I, Gillespie R.J, Tang T.H., Bader R.F. Inorganic Chemistry, 34,9, 2407–2414, 1995 doi:10.1021/ic00113a023
- ^ Power, Philip P. Silicon, germanium, tin and lead analogues of acetylenes. Chem. Commun. September 2003, (17): 2091–2101. PMID 13678155. doi:10.1039/B212224C.
- ^ Nagase, Shigeru; Kobayashi, Kaoru; Takagi, Nozomi. Triple bonds between heavier Group 14 elements. A theoretical approach. J. Organomet. Chem. 6 October 2000, 11 (1–2): 264–271. doi:10.1016/S0022-328X(00)00489-7.
- ^ Sekiguchi, Akira; Kinjō, Rei; Ichinohe, Masaaki. A Stable Compound Containing a Silicon–Silicon Triple Bond (PDF). Science. September 2004, 305 (5691): 1755–1757. Bibcode:2004Sci...305.1755S. PMID 15375262. S2CID 24416825. doi:10.1126/science.1102209.[永久失效链接]
- ^ A spectroscopic determination of the bond length of the LiOLi molecule: Strong ionic bonding, D. Bellert, W. H. Breckenridge, J. Chem. Phys. 114, 2871 (2001); doi:10.1063/1.1349424
- ^ Wells A.F. (1984) Structural Inorganic Chemistry 5th edition Oxford Science Publications ISBN 978-0-19-855370-0
- ^ Housecroft, C. E.; Sharpe, A. G. Inorganic Chemistry 2nd. Prentice Hall. 2004. ISBN 978-0130399137.
