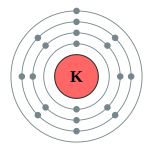
鉀
鉀(英語:Potassium)是一種化學元素,化學符號為K(源於拉丁語:Kalium),原子序數為19,原子量為39.0983 u。[3]
鉀最早於植物的灰燼中所分離出,故其名稱源自植物的灰燼(英語:pot ash)。在元素週期表中,鉀屬於鹼金族,所有鹼金屬在外部電子殼中都具有單價電子在離子鹽中發生。其易被去除電子而形成具有正電荷的離子──陽離子(陽離子可與陰離子結合形成鹽)。
鉀元素在自然界裏僅以離子化合物存在,是一種柔軟的銀白色鹼性金屬。在空氣中會迅速氧化,遇水會劇烈反應,產生足夠的熱量以點燃反應中釋放的氫氣,並放出藍紫色的火焰。它被發現溶解於海水(自然界中的鉀以化合物的形式溶解於海水中,按重量百分比計為0.04%[4][5]),是許多礦物質的一部分。
鉀與鈉的化學性質非常相似,而鈉是元素週期表第1族中鉀的前一個元素。它們具有相似的第一電離能,讓原子丟棄其最外層唯一的電子。在1702年[6],鉀與鈉被懷疑可以與相同的陰離子結合形成類似的鹽類,並且在1807年以電解證明。天然存在的鉀由三種同位素組成,其中的40
K是放射性的。微量的40
K存在於所有鉀中,它是人體中最常見的放射性同位素。
鉀離子對所有活細胞的功能非常重要。正常的神經傳遞需要鉀離子通過神經細胞膜轉移;過低或過量的鉀也都會導致許多身體的徵兆或症狀,包括心律異常和各種心電圖異常。新鮮水果和蔬菜是鉀的良好來源。身體攝取鉀時,血漿中的鉀離子濃度會上升,造成鉀離子從細胞外往細胞內移動,增加腎臟對鉀離子的代謝。
鉀的大多數工業應用了鉀化合物(例如鉀皂)在水中的的高溶解度。含鉀的農業肥料佔了全球鉀化學產物的95%,用於補救因大量生產作物而耗盡鉀的土壤。 [7]
性質
[編輯]鉀的熔點、硬度低,比鈉更活潑,在空氣中很快氧化。鉀的密度小於水,大於煤油。鉀和水會產生劇烈反應(產生高溫使自己熔成一個銀白色的球,釋放大量氫,使金屬球在水面高速移動,氫氣燃燒,可以看到紫藍色的火焰,生成氫氧化鉀。方程式如下:
鉀可以和鹵族、氧族元素反應,還可以使其他金屬的鹽類還原(熔融狀態下),對有機物有很強的還原作用。
發現
[編輯]1807年由英國化學家戴維首次用電解法從熔融氫氧化鉀中製得金屬鉀,並定名。
名稱由來
[編輯]拉丁語:kalium,這個單字不存在於古典拉丁語中,這是由永斯·貝采利烏斯創造的新拉丁文名詞。這個名詞起源於阿拉伯語:القَلْيَه(al-qalyah),本義為植物灰燼。qaly是刺沙蓬一類的植物,古人焚燒這種植物,從灰燼中可以的得到不純的鉀鹽和鈉鹽混合物,進而和石灰水反應可以得到強鹼溶液。這個阿拉伯名詞傳入歐洲後,被拼為alkali,意為鹼。永斯·貝采利烏斯以此命名鉀為kalium。
鉀英文名「potassium」則由「Potash」衍生而來。當時的人們焚燒木材,其灰燼用水浸泡,取上清液,在銅鍋里煮沸除去水分,可得不純的鉀鹽混合物,稱為草木灰(英語:Potash,Pot-Ashes:pot鍋,ash灰燼,譯作「草木灰」)。戴維使用的氫氧化鉀就是從草木灰轉化而來的,因此將鉀命名為potassium。
分佈
[編輯]鉀在自然界中只以化合物形式存在。在雲母、鉀長石等矽酸鹽中都富含鉀。鉀在地殼中的含量約為2.09%,居第七位。在海水中以鉀離子的形式存在,含量約為0.1%。鉀在海水中含量比鈉離子少的原因是由於被土壤和植物吸收多。在動植物體內也含有鉀。正常人體內約含鉀175克,其中98%的鉀貯存於細胞液內,是細胞內最主要的陽離子。
製備
[編輯]這種元素通過將其常見的氫氧化物進行電解而得到。將氫氧化鉀與鹵化物進行熔融電解,再經真空蒸餾製得。 早期,由法國化學家給呂薩克和泰納爾發明的隔絕空氣加強熱於碳酸鉀、碳粉、鐵粉、明礬混合物的方法也被用於製備粗鉀,並被用於當時的一種打火機中。
同位素
[編輯]已發現的鉀的同位素共有16種,包括鉀35至鉀50,其中只有鉀39和鉀41是穩定的,其他同位素都帶有放射性。
應用
[編輯]鉀主要用作還原劑及用於合成中。鉀的化合物在工業上用途很廣。鉀鹽可以用於製造化肥及肥皂。鉀對動植物的生長和發育起很大作用,是植物生長的三大營養元素之一。
鉀金屬在工業上可作為較強的還原劑。鈉鉀合金在一些特殊冷卻設備中作為熱傳導的媒介。
對人體的影響
[編輯]營養代謝
[編輯]鉀是人體必需的礦物質營養素,是體細胞內主要的陽離子,體重70公斤的成年男性體內,鉀含量約3500mEq。飲食中的鉀離子在小腸中很容易被吸收。人體鉀離子主要流失途徑有80-90%是由腎臟經尿液排除,其餘10-20%是由糞便排出。腎臟對於鉀離子具有調控作用,藉以維持鉀離子濃度在正常範圍內。基於彌補身體的流失量以維持正常儲存及血漿濃度的平衡,成人每日的最小需要量為200 mg。含鉀豐富的食物 (頁面存檔備份,存於互聯網檔案館)包括乳製品、水果、蔬菜、瘦肉、內臟、香蕉、葡萄乾、金槍魚、菠菜、鱷梨、酸奶、鮭魚、石榴、扁豆、蘑菇、牛奶[8]等。飲食建議攝取量如下:
| 鉀充足攝取量 (公克/天) |
| 0.4 |
| 0.7 |
| 3.0 |
| 3.8 |
| 4.5 |
| 4.7 |
| 4.7 |
| 5.1 |
鉀可以調節細胞內適宜的滲透壓和體液的酸鹼平衡,參與細胞內糖和蛋白質的代謝。有助於維持神經健康、心跳規律正常,可以預防中風,並協助肌肉正常收縮。在攝入高鈉而導致高血壓時,鉀具有降血壓作用。細胞對鉀的調節與鈉鉀泵(Na+/K+ pump)和鉀離子通道有關。
低血鉀(Hypokalemia)
[編輯]人體鉀缺乏可引起心跳不規律和加速、心電圖異常、肌肉衰弱和煩躁,最後導致心跳停止。一般而言,身體健康的人,會自動將多餘的鉀排出體外。但腎病患者則要特別留意,避免攝取過量的鉀。
導致低血鉀的原因包括:長期嘔吐、腹瀉、糖尿病酸中毒、神經性厭食症、長期營養不良、慢性酒精中毒、腎上腺腫瘤、燙傷、臨床上常見的電解質異常、吸收不良或血鉀過度流失、或使用某些藥物而使血中之鉀濃度不夠。輕度低血鉀(血清鉀濃度3.0-3.5meq/L)經常是沒有症狀;中度低血鉀(血清鉀濃度2.5-3.0meq/L)有非特異性的症狀像是虛弱、疲倦、便秘等;嚴重低血鉀(血清鉀濃度<2.5meq/L)可能發生肌肉壞死,甚至呼吸肌麻痺衰竭。補充鉀離子是治療低血鉀的最根本辦法。[10][11]
高血鉀(Hyperkalemia)
[編輯]血中鉀離子濃度高於5.5 mEq/L時稱為高血鉀,可能因攝取過多、排泄減少、或因鉀離子由細胞內轉移至細胞外液等原因造成。一般以腎臟衰竭病患容易發生高血鉀。當人體發生高血鉀時,會有血壓降低、心律不整、心電圖改變、嚴重時會有心室纖維顫動、心跳停止。神經肌肉的症狀在早期為肌肉震顫、痙攣、感覺異常等情形,晚期則會有肌肉無力、弛緩性麻痺、呼吸停止。此外也會出現噁心、嘔吐、腸蠕動增加、腹瀉、腹絞痛等消化系統的症狀及少尿、無尿等泌尿系統的症狀。[10]
相關遺傳性疾病
[編輯]- 家族性低血鉀週期性無力症(familial hypokalemic periodic paralysis),為自體顯性遺傳疾病,相當罕見。突變的基因CACNL1A3是一種鈣離子通道。疾病的特徵是突然發生的肌肉麻痺與血清鉀濃度<2.5meq/L。血鉀減少的原因可能是大量攝取碳水化合物或鈉離子而誘發,會在24小時內自然消退,但有時會引起致命性心率不整[12]。
- 李德爾氏綜合徵(Liddle's syndrome)為隱性遺傳疾病。此遺傳異常會因為礦物皮質醛酮增高,影響到腎臟離子輸送活性,刺激集尿管細胞對鈉離子的再吸收,造成代謝性鹼中毒和低血鉀。
- 巴特氏症候群(Bartter's syndrome)為亨利氏環(loop of Henle)和近曲小管的鈉運輸蛋白(chloride-associated sodium transporters)失去活性或功能[13]。
- 吉特曼氏綜合症(Gitelman's syndrome)是腎臟遠曲小管(distal convoluted tubule)鈉運輸蛋白失去活性或功能。
參考資料
[編輯]- ^ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. Standard atomic weights of the elements 2021 (IUPAC Technical Report). Pure and Applied Chemistry. 2022-05-04. ISSN 1365-3075. doi:10.1515/pac-2019-0603 (英語).
- ^ Magnetic susceptibility of the elements and inorganic compounds (頁面存檔備份,存於互聯網檔案館), in Lide, D. R. (編), CRC Handbook of Chemistry and Physics 86th, Boca Raton (FL): CRC Press, 2005, ISBN 0-8493-0486-5
- ^ 夏征農、陳至立 (編). 《辞海》第六版彩图本. 上海: 上海辭書出版社. 2009年: 第3227頁. ISBN 9787532628599.
- ^ Webb, D. A. The Sodium and Potassium Content of Sea Water (PDF). The Journal of Experimental Biology. April 1939, (2): 183 [2019-02-22]. (原始內容 (PDF)存檔於2019-09-24).
- ^ Anthoni, J. Detailed composition of seawater at 3.5% salinity. seafriends.org.nz. 2006 [2011-09-23]. (原始內容存檔於2019-01-18).
- ^ Marggraf, Andreas Siegmund. Chymische Schriften. 1761: 167 [2019-02-22]. (原始內容存檔於2021-04-29).
- ^ Greenwood, p. 73
- ^ WebMD 網醫生. 含钾高的食物一览表,富含钾的蔬菜,富含钾的食物和水果. WebMD. 2019-01-16. (原始內容存檔於2021-04-17).
- ^ Institute of Medicine(2005)Dietary Reference Intakes for Water, Potassium, Sodium, Chloride, and Sulfate. pp. 186-268. National Academy Press, ISBN 978-0-309-53049-1
- ^ 10.0 10.1 長庚生物科技股份有限公司. www.cgb.com.tw. [2007-12-22]. (原始內容存檔於2021-04-15).
- ^ 存档副本. [2007-12-22]. (原始內容存檔於2007-11-04).
- ^ 存档副本. [2007-12-22]. (原始內容存檔於2017-07-30).
- ^ [1][永久失效連結]
外部連結
[編輯]- 元素鉀在洛斯阿拉莫斯國家實驗室的介紹(英文)
- EnvironmentalChemistry.com —— 鉀(英文)
- 元素鉀在The Periodic Table of Videos(諾丁漢大學)的介紹(英文)
- 元素鉀在Peter van der Krogt elements site的介紹(英文)
- WebElements.com – 鉀(英文)