乙二醇
外观
此条目需要扩充。 (2011年5月21日) |
| 乙二醇 | |
|---|---|

| |
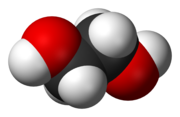
| |
| IUPAC名 Ethane-1,2-diol 1,2-乙二醇 | |
| 别名 | 甘醇 水精 |
| 识别 | |
| 缩写 | MEG |
| CAS号 | 107-21-1 |
| PubChem | 174 |
| ChemSpider | 13835235 |
| SMILES |
|
| InChI |
|
| InChIKey | LYCAIKOWRPUZTN-UHFFFAOYAD |
| Beilstein | 505945 |
| Gmelin | 943 |
| 3DMet | B00278 |
| EINECS | 203-473-3 |
| ChEBI | 30742 |
| RTECS | KW2975000 |
| KEGG | C01380 |
| MeSH | Ethylene+glycol |
| 性质 | |
| 化学式 | C2H4(OH)2 |
| 摩尔质量 | 62.068 g·mol⁻¹ |
| 密度 | 1.1132 g·cm-3 |
| 熔点 | −12.9 °C (8.8 °F) |
| 沸点 | 197.3 °C (387 °F) |
| 溶解性(水) | 任意比例互溶 |
| 危险性 | |
| 闪点 | 111 °C (closed cup) |
| 自燃温度 | 410 °C |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
乙二醇,又名甘醇、水精。化学式为HOCH2—CH2OH。属于最简单的二元醇。无色无臭、有甜味液体,能与水以任意比例混合。用作溶剂、防冻剂以及PETE等的原料。乙二醇是化纤产业的基础原料之一。
乙二醇对动物有毒性,人类致死剂量估计为1.6 g/kg,[1]不过成人服食30毫升已有可能引致死亡。[2]
制备
[编辑]乙二醇可由乙烯透过反应中间体环氧乙烷产生。环氧乙烷与水的反应产生乙二醇的化学反应式如下:
- C2H4O + H2O → HO–CH2CH2–OH
此反应可由酸或碱的催化下加速反应,或在中性pH值条件下提高的温度也可以加速反应。乙二醇最高的产率发生在酸性或中性pH下与大量过量的水,在这条件下,乙二醇的产量可达90%。主要的副产物是属于乙二醇低聚物的二甘醇、三甘醇及四甘醇。每年生产约六十七亿公斤。 有一个选择性较高的方式是使用OMEGA process。反应式为:
- C2H4O + CO2 → C3H4O3
- C3H4O3 + H2O → HOC2H4OH + CO2
在OMEGA process中,
- 第一步骤:环氧乙烷先与二氧化碳转变成碳酸乙烯酯(Ethylene carbonate)。
- 第二步骤:碳酸乙烯酯与水反应,选择性地产生乙二醇单体。在第二步骤被释放的二氧化碳,可以回馈到第一步骤再使用。[3]
毒性
[编辑]相较于甲醇的最低致死剂量(LDLO)为1-2毫克/公斤,乙二醇的毒性不高,目前已知对人类的最低致死剂量为786毫克/公斤。[4]乙二醇最大的危险性在于它的甜味。因此相较于其他有毒物质,孩童和动物比较容易因摄取大量的乙二醇而中毒。经过消化系统作用,乙二醇会先被氧化成乙醇酸,再被氧化成草酸。乙二醇及其副产物会先影响中枢神经系统,接着是心脏,而后影响肾脏。如无适当治疗,摄取过量乙二醇会导致死亡。[5]
根据美国毒物管制中心2007年的资料,当年有大约1000起乙二醇中毒事件且其中有16人死亡。2008年则有7人死于乙二醇中毒。[6]
生活环境中的乙二醇
[编辑]- 生活环境中的乙二醇主要来自于机场的用来除冰的除冰剂、车辆冷却系统的防冻剂(水箱水、水箱精,现在部分改用不具毒性的1,2-丙二醇)或其他含有乙二醇的产品。
- 乙二醇在大气中自然分解的时间大约为10天。
- 水中或土壤中的乙二醇则需大约几个星期才会分解。[7]
参考资料
[编辑]- ^ 存档副本. [2007-09-02]. (原始内容存档于2007-09-28).
- ^ Field D. Acute ethylene glycol poisoning. Crit Care Med. 1985, 13 (10): 872–3. PMID 4028762.
- ^ Siegfried Rebsdat; Dieter Mayer (2005), "Ethylene Glycol", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi: 10.1002/14356007.a10_101
- ^ Safety Officer in Physical Chemistry. Safety (MSDS) data for ethylene glycol. Oxford University. November 23, 2009 [December 30, 2009]. (原始内容存档于2011-12-14).
- ^ Ethylene glycol (页面存档备份,存于互联网档案馆). National Institute for Occupational Safety and Health. Emergency Response Database. August 22, 2008. Retrieved December 31, 2008.
- ^ (Toxicity, Ethylene Glycol). [2012-05-02]. (原始内容存档于2012-04-20).
- ^ (CDC ToxFAQs). [2012-05-02]. (原始内容存档于2012-05-05).
外部链接
[编辑]查看维基词典中的词条“Ethylene glycol”。
- ГОСТ 19710-83. Этиленгликоль. Технические условия.(页面存档备份,存于互联网档案馆) (俄文)
- Hairong Yue, Yujun Zhao, Xinbin Ma and Jinlong Gong. Ethylene glycol: properties, synthesis, and applications. Critical Review(页面存档备份,存于互联网档案馆) — Chemical Society Reviews. Issue 11, 2012, 41, 4218-4244. DOI: 10.1039/C2CS15359A (英文)
