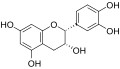
儿茶素
此条目需要补充更多来源。 (2024年5月3日) |
| 儿茶素 | |
|---|---|

| |
| IUPAC名 (2R,3S)-2-(3,4-dihydroxyphenyl)-3,4-dihydro-2H-chromene-3,5,7-triol | |
| 英文名 | Catechin |
| 识别 | |
| CAS号 | 7295-85-4(±) 154-23-4(+) 18829-70-4(-) 88191-48-4((+)、水合物) |
| PubChem | 9064 |
| ChemSpider | 8711 |
| SMILES |
|
| InChI |
|
| InChIKey | PFTAWBLQPZVEMU-DZGCQCFKBX |
| ChEBI | 15600 |
| 性质 | |
| 化学式 | C15H14O6 |
| 摩尔质量 | 290.27 g·mol−1 |
| 外观 | 无色固体 |
| 熔点 | 175—177 °C(347—351 °F;448—450 K) |
| λmax | 276 nm |
| [α]20 D |
+14.0° |
| 危险性 | |
| 警示术语 | R:R36/37/38 |
| 安全术语 | S:S26-S36 |
| 主要危害 | 哺乳动物体细胞、细菌、酵母的突变原 |
| 致死量或浓度: | |
LD50(中位剂量)
|
(+)-儿茶素:10,000 mg/kg(大鼠)(RTECS) 10,000 mg/kg(小鼠) 3,890 mg/kg(大鼠)(其它来源) |
| 药理学 | |
| 给药途径 | 口服 |
| 药代动力学: | |
| 尿液 | |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
儿茶素(catechin)又称儿茶酸[1](catechuic acid[2])、西阿尼醇(cianidanol[3]),是多羟基黄烷-3-酚的总称,含2,3–位构型不相同的4个异构体,属于黄烷醇类物质。可由儿茶中提取,为无色结晶形固体,能溶于水。
儿茶素可从茶(Camellia sinensis)的全株等多种植物中分离得到,是茶多酚中最重要的一种,约占茶多酚含量的75%到80%,也是茶的苦涩味的来源之一,具有抗氧化作用[4] [5]。其与咖啡因同属茶叶中的两大重要机能性成分,可增强新陈代谢,增加脂肪氧化供能。
儿茶素主要分为四种:表儿茶素(epicatechin,EC)、表没食子儿茶素(epigallocatechin,EGC)、表儿茶素没食子酸酯(epicatechin gallate,ECG)和表没食子儿茶素没食子酸酯(epigallocatechin gallate,EGCG)。
儿茶素是黄烷-3-醇,一种天然苯酚和抗氧化剂。它是一种植物次生代谢产物。它属于基团黄烷-3-醇类(黄烷醇),黄酮类化合物化学家族的一部分。儿茶素化学家族的名字从儿茶取得,这是含羞草属儿茶或金合欢儿茶的汁或水煮提取物。
而人体常见的激素儿茶酚胺是具有儿茶酚核的(苯乙)胺类化合物的统称,是由肾上腺产生的一类应激拟交感“斗或逃”(fight or flight)激素。最重要的儿茶酚胺是肾上腺素、去甲肾上腺素(正肾上腺素)和多巴胺,均是从苯丙氨酸和酪氨酸合成。不少精神兴奋剂也是儿茶酚胺的类似物[6]。
化学
[编辑]
|

|

|
| 黄酮类化合物的编号 | (+)–儿茶素的编号 | guibourtinol |
儿茶素具有两个苯环(A和B环)和二氢吡喃杂环(C环)其上的碳3为羟基。A环是类似于间苯二酚部分而B环是类似于儿茶酚部分。有两个手性中心在碳原子2和3。因此,它有四个非对映异构。异构体的两个处于反式构型,被称为儿茶素和另外两个是在顺式构型,被称为表儿茶素。最常见的儿茶素异构体是(+)–儿茶素。另一立体异构体是(-)–儿茶素。最常见的表儿茶素异构体是(-)–表儿茶素。不同的差向异构体可以使用手性柱色谱进行区分。
- 立体异构体
-
(+)-儿茶素 (2R,3S)
-
(-)-儿茶素 (2S,3R)
-
(-)-表儿茶素 (2R,3R)
-
(+)-表儿茶素 (2S,3S)
自然产生
[编辑](+)– 儿茶素和(-)–表儿茶素以及它们的没食子酸结合物在维管束植物无处不在,和传统草药,如中国药植嘴叶钩藤等常见的组成部分。这两种异构体大多在可可和茶的成分中发现。( - )–表儿茶素可以在可可豆中找到,首先称可可醇。这是从绿茶通过美智代在1929年分离出来。 在1931年马克西米利安证明儿茶素存在可可豆中。 儿茶素还发现作为苷和糖苷形式还具有抗氧化性能。
食品成分
[编辑]在欧洲和美国的儿茶素类的主要膳食来源是茶与仁果类水果。儿茶素和表儿茶素在可可,儿茶素类的含量(108毫克/100克),接着西梅汁(25毫克/ 100毫升)和蚕豆荚(16毫克/ 100克)。巴西莓果油含有儿茶素(67毫克/千克。表儿茶素和 儿茶素是摩洛哥坚果油的主要天然酚。儿茶素在各不相同食物中,从桃子绿茶和醋均有。儿茶素是大麦主要的酚类化合物负责面团变色。
代谢
[编辑]生物合成
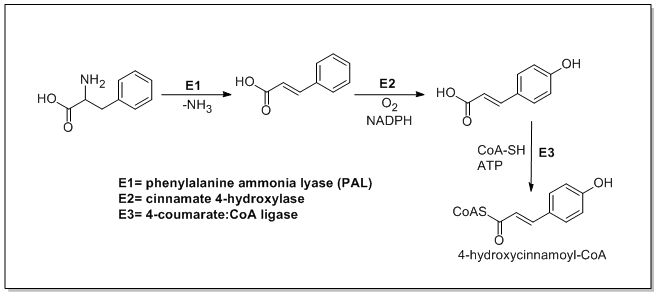
[编辑]儿茶素的植物生物合成始于4-羟基肉桂酰辅酶A,通过一个聚酮合酶3途径(PKSIII途径)加入三个丙二酰辅酶A,形成链的延伸。4-羟基肉桂酰辅酶A是由L-苯丙氨酸通过莽草酸途径生物合成。L-苯丙氨酸首先由苯丙氨酸氨裂解酶(PAL)的脱氨基形成肉桂酸,然后由肉桂酸-4-羟化酶氧化为4-羟基肉桂酸。然后查耳酮合酶催化4-羟基肉桂酰辅酶A的缩合和丙二酰-辅酶A的三个分子形成查尔酮(chalcone)。然后由查尔酮异构酶将查耳酮异构化成柚皮素,它由类黄酮3'羟化酶氧化成圣草酚和进一步氧化黄烷酮由3羟化酶到花旗松。然后由二氢黄烷醇-4-还原酶将花旗松素还原,然后由无色花色素还原酶还原产生儿茶素。儿茶素的生物合成如下所示。
无色花青素还原酶(LCR)使用2,3-反式 - 3,4-顺式无色花青素,以产生(+)–儿茶素和是在原花色素的第一种酶(PA)的专用通道。其活性在叶,花和种子已经过测量,如豆科植物紫花苜蓿,百脉根,莲花,岩黄芪属和刺槐。所述酶也存在于葡萄。

生物降解
[编辑]
儿茶素加氧酶是儿茶素降解的关键酶,存在于真菌和细菌中。在细菌之间降解(+)–儿茶素可以通过醋酸钙不动杆菌来实现。儿茶素代谢成原儿茶酸和间苯三酚羧酸。它也可由大豆慢生根瘤菌降解。间苯三酚羧酸进一步脱羧成间苯三酚,这是脱羟基化成间苯二酚。间苯二酚被羟化成羟基喹啉。原儿茶酸和羟基喹啉进行内部二醇裂解 通过儿茶酸3,4-双加氧酶和羟基喹啉1,2-双加氧酶,以形成β羧基顺,顺 - 己二烯二酸和乙酸顺丁烯二酰基。
真菌之间,儿茶素的降解可通过角毛壳菌来实现。
人类
[编辑]儿茶素类是从胃肠道经摄取,特别是空肠,及在肝中,产生所谓的结构相关的表儿茶素代谢物(SREM)。对于结构相关的表儿茶素代谢物主要代谢途径由儿茶酚-O-甲基转移酶由葡糖醛酸化,硫酸化及甲基化儿茶酚组,血浆仅检测出微量。大多数饮食儿茶素类由结肠肠道微生物代谢成伽马–戊内酯及马尿酸并且经过肝脏中葡萄糖醛酸化,硫酸化和甲基化进一步的生物转化。
关于儿茶素类的立体化学构造对它们的摄取及代谢产生巨大影响,摄取最高的为(-)–表儿茶素而最低的为(-)–儿茶素。
生物活性研究
[编辑]血管功能
[编辑]几个世纪前含儿茶素的提取液被认为有用于治疗心脏疾病,和于1936年发现对毛细血管的通透性产生影响。从膳食研究有限的证据表明,儿茶素可能对内皮依赖性血管舒张产生影响,这可能在人类中有助于正常的血流调节。绿茶中的儿茶素可改善高血压,尤其是当收缩压超过130毫米汞柱时。由于在消化过程中广泛代谢,负责对血管的这种效果的儿茶素代谢物的命运和活动,以及作用的实际模式未知
欧洲食品安全局确定了可可黄烷醇对健康成人血管功能的作用 它通过了结论:可可黄烷醇帮助维持内皮依赖性血管舒张,这有助于正常血液流动。从观察队列研究的数据并没有显示出黄烷-3-醇摄取和心血管疾病的风险之间的一致的关联性。
荟萃分析还表明,绿茶中的儿茶素可有利影响胆固醇。
可能的免疫效果
[编辑]视摄取量而定,儿茶素及其代谢物可与红血球细胞结合,此结合可能诱导自体抗原释出,造成溶血性贫血或肾衰竭。此发现导致用于治疗病毒性肝炎的药品“Catergen”被召回。
对植物的影响
[编辑]有些植物会释放儿茶素到地面,可能会阻碍他们的邻居植物的生长,这是相生相克的一种形式。
注释
[编辑]- ^ 國家教育研究院-化學名詞-有機化合物學術名詞. 国家教育研究院.
- ^ Cianidanol. PubChem.
- ^ Martin Negwer. Organic-chemical Drugs and Their Synonyms 7. Akad.-Verlag. 1994: 991. ISBN 9783055016295.
- ^ Cutch and catechu plant origin. Food and Agriculture Organization of the United Nations. 5 November 2011 [2019-02-19]. (原始内容存档于2019-02-10).
- ^ 李宁,陈伟主编. 全民健康安全知识丛书 保健食品安全知识读本. 北京:中国医药科技出版社. 2017.03: 126. ISBN 978-7-5067-9042-0.
- ^ 阚建全主编. 食品化学. 北京:中国农业大学出版社. 2016.08: 282. ISBN 978-7-5655-1597-2.