组蛋白乙酰化
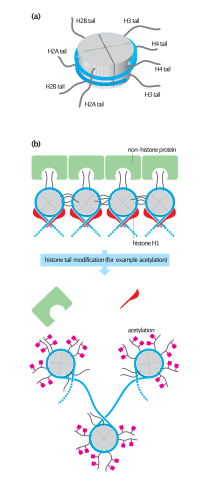
(a)核小体示意图,可见组蛋白的N端向外延伸
(b)组蛋白未被乙酰化的状态,其N端与周围的组蛋白或其他蛋白(绿色结合),染色体包裹较紧密
(c)组蛋白被乙酰化的状态,染色体包裹较松散,有利于基因表现
组蛋白乙酰化(Histone acetylation)为真核生物染色体上包裹DNA的组蛋白N端之离胺酸被乙酰化的转译后修饰,为细胞调控基因表现的一种机制。此反应一般由组蛋白乙酰转移酶(HAT)催化,组蛋白脱乙酰酶(HDAC)则可催化其逆反应组蛋白脱乙酰化( Histone deacetylation),将组蛋白上的乙酰基水解移除[1]。组蛋白乙酰化是为一种表观遗传修饰,乙酰基化会消除组蛋白离胺酸所带的正电荷,使其与DNA(带负电)的结合力降低[2],因此可将原本缠绕较紧密的染色体结构(异染色质)转成较疏松的型态(真染色质),有利于转录的进行而提升基因表现;组蛋白脱乙酰化的功能则与之相反,可使染色体结构变得更紧密而降低基因表现[3][4]。
组蛋白上不同位点的多种修饰(包括乙酰化、甲基化、磷酸化等)可能组合成组蛋白密码,共同影响染色体结构,并与细胞中的其他蛋白结合以调控基因的转录[5][6],例如具有布罗莫结构域的蛋白(包括许多转录因子)可与被乙酰化的组蛋白结合[7] 。组蛋白密码与DNA甲基化皆为表观遗传密码的一部份[8]。
组蛋白乙酰化调控许多基因的表现,因此其调控异常与发炎性疾病、心血管疾病、神经性疾病和多种癌症相关[9][10]。此外对烟酒和药物的成瘾机制可能也与其促进染色体特定区域的组蛋白乙酰化以影响基因表现有关[11][12]。
参考文献[编辑]
- ^ Grunstein M. Histone acetylation in chromatin structure and transcription (PDF). Nature. September 1997, 389 (6649): 349–52 [2021-04-24]. Bibcode:1997Natur.389..349G. PMID 9311776. doi:10.1038/38664. (原始内容存档 (PDF)于2016-03-03).
- ^ Watson, James D.; Baker, Tania A.; Gann, Alexander; Levine, Michael; Losik, Richard. Molecular biology of the gene Seventh. Boston: Pearson/CSH Press. 2014. ISBN 978-0-321-76243-6.
- ^ Struhl K. Histone acetylation and transcriptional regulatory mechanisms. Genes & Development. March 1998, 12 (5): 599–606. PMID 9499396. doi:10.1101/gad.12.5.599.
- ^ de Ruijter AJ, van Gennip AH, Caron HN, Kemp S, van Kuilenburg AB. Histone deacetylases (HDACs): characterization of the classical HDAC family. The Biochemical Journal. March 2003, 370 (Pt 3): 737–49. PMC 1223209
 . PMID 12429021. doi:10.1042/BJ20021321.
. PMID 12429021. doi:10.1042/BJ20021321.
- ^ Chi P, Allis CD, Wang GG. Covalent histone modifications--miswritten, misinterpreted and mis-erased in human cancers. Nature Reviews. Cancer. July 2010, 10 (7): 457–69. PMC 3262678
 . PMID 20574448. doi:10.1038/nrc2876.
. PMID 20574448. doi:10.1038/nrc2876.
- ^ Barratt MJ, Hazzalin CA, Cano E, Mahadevan LC. Mitogen-stimulated phosphorylation of histone H3 is targeted to a small hyperacetylation-sensitive fraction. Proceedings of the National Academy of Sciences of the United States of America. May 1994, 91 (11): 4781–5. Bibcode:1994PNAS...91.4781B. PMC 43872
 . PMID 8197135. doi:10.1073/pnas.91.11.4781.
. PMID 8197135. doi:10.1073/pnas.91.11.4781.
- ^ Sanchez R, Zhou MM. The role of human bromodomains in chromatin biology and gene transcription. Current Opinion in Drug Discovery & Development. September 2009, 12 (5): 659–65. PMC 2921942
 . PMID 19736624.
. PMID 19736624.
- ^ Jenuwein T, Allis C. Translating the histone code. Science. 2001, 293 (5532): 1074–80. PMID 11498575. doi:10.1126/science.1063127.
- ^ Barnes PJ, Adcock IM, Ito K. Histone acetylation and deacetylation: importance in inflammatory lung diseases. The European Respiratory Journal. March 2005, 25 (3): 552–63. PMID 15738302. doi:10.1183/09031936.05.00117504.
- ^ Glozak MA, Seto E. Histone deacetylases and cancer. Oncogene. August 2007, 26 (37): 5420–32. PMID 17694083. doi:10.1038/sj.onc.1210610.
- ^ Robison AJ, Nestler EJ. Transcriptional and epigenetic mechanisms of addiction. Nature Reviews. Neuroscience. October 2011, 12 (11): 623–37. PMC 3272277
 . PMID 21989194. doi:10.1038/nrn3111.
. PMID 21989194. doi:10.1038/nrn3111.
- ^ Hitchcock LN, Lattal KM. Histone-mediated epigenetics in addiction. Epigenetics and Neuroplasticity—Evidence and Debate. Progress in Molecular Biology and Translational Science 128. 2014: 51–87. ISBN 9780128009772. PMC 5914502
 . PMID 25410541. doi:10.1016/B978-0-12-800977-2.00003-6.
. PMID 25410541. doi:10.1016/B978-0-12-800977-2.00003-6. |journal=被忽略 (帮助)
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
